当科では、データベースを活用した様々な臨床研究と、動物モデルやヒト臨床サンプルなどを使った基礎研究を、どちらも積極的に行っています。膠原病学や免疫学の臨床・基礎研究に興味のある皆様の参加をお待ちしています。

臨床研究
関節リウマチに関する臨床研究
私たちは、関節リウマチの疾患データベースとして、京都大学、大阪大学、大阪医科大学、関西医科大学、神戸大学、奈良県立医科大学などとともに、関西多施設ANSWERコホートを立ち上げ活動しています。従来の大規模コホートでは疾患活動性データの登録が年1-2回のところ、ANSWERコホートには11,624名のRA患者ののべ145,627件の縦断的な疾患活動性データが登録されており、薬剤の奏効性を含めた様々な解析が可能となっています。当科は当院の整形外科リウマチ科とも密接に連携しており、ANSWERコホートにも内科・整形外科で一緒に参加しています。このように、診療科や大学の垣根を越えて、様々な先生方と力を合わせながら共同研究をすすめていくという、臨床研究の醍醐味を経験することができます。これまでに様々な診療科と一緒に、歯周病やサルコペニア、睡眠、薬物アドヒアランス、不安うつなどRA患者のADL/QOLにかかわる共同研究も行ってきました。また、ANSWERコホートを活用した当科主導のRA患者のサルコペニアと運動療法に関する臨床研究が、2020年度のAMED研究課題として採択されています。

- 1) Hashimoto M, et al. Arthritis Res Ther. 2019
- 2) Ebina K, Hashimoto M. et al. PLoS One. 2019
- 3) Jinno S, et al. Rheumatol Int. 2020
- 4) Hashimoto M, et al. PLoS One. 2015
- 5) Torii M. Hashimoto M. et al. Mod Rheumatol. 2019
- 6) Hamamoto K, Yamada S, et al. Am J Hypertens. 2016
SLEに関する臨床研究
SLEは膠原病の中でも最も病態が多様であり、病態の適切な評価基準や患者の層別化が困難であったために、各種治験薬が臨床試験の最終段階で目標を達成できず撤退を余儀なくされるという、いわゆる「膠原病創薬の壁」に阻まれてきた疾患です。最近ようやくいくつかの有望な治療薬がその壁を乗り越え使用可能となってきましたが、今後はそれらの治療薬が実臨床の患者さんのどのような病態に最も有効なのか、ということを実臨床のデータをもって明らかにしていく必要があります。すなわち、SLEは現在特にデータベース化が求められている疾患といえます。当科は、関節リウマチでこれまで培ってきた経験を生かしてSLEの疾患コホートを構築しています。SLEの疾患コホート構築においても多施設の先生方と積極的に連携していきたいと思います。
血管炎に関する臨床研究
多施設共同研究
当科は、厚生労働省の「難治性血管炎の医療水準・患者QOL向上に資する研究班(研究代表者:東京女子医科大学 針谷正祥教授)」に参加し、血管炎診療ガイドラインの改訂に参加しています。当研究班では、ANCA血管炎に関する最先端のエビデンスについて、システマチック・レビューを行い、さらにメタ解析を行うことで、2017年版のANCA関連血管炎診療ガイドラインの改訂を行っています。
自施設における研究
当科では、高安動脈炎・巨細胞性動脈炎・ANCA関連血管炎など、血管炎の患者さんに対する診療を積極的に行っております。お困りの患者さんや治療を相談したい患者さんなどがおりましたら、お気軽にご紹介ください。
- 1) 大血管炎95例の後方視的解析(Yoshida M, Watanabe R, et al. Int J Rheum Dis. 2016)
- 2) 高安動脈炎に合併する潰瘍性大腸炎について(Watanabe R, et al. Mod Rheumatol. 2014)
その他の膠原病・稀少疾患に関するコホート研究
関節リウマチやSLE、血管炎のみならず、当科では、多くの膠原病や稀少疾患も積極的に診断治療を行っています。そういった患者さんを後方視的に解析し、積極的に発表しています。
経験を積みたい先生は、症例報告のみならず、そういったコホート研究を行って頂くことも可能です。
- 1) PMR 89例の再発に関する因子(Okazaki S, Watanabe R, et al. Tohoku J Exp Med. 2020)
- 2) PM/DM 124例の予後因子の解析(Ishizuka M, Watanabe R, et al. Mod Rheumatol. 2016)
- 3) 強皮症139例の間質性肺炎の解析(Tomiyama F, Watanabe R, et al. Tohoku J Exp Med. 2016)
基礎研究
動物モデルを用いた膠原病の病態解明
関節リウマチ・SLE・脊椎関節炎の動物モデル
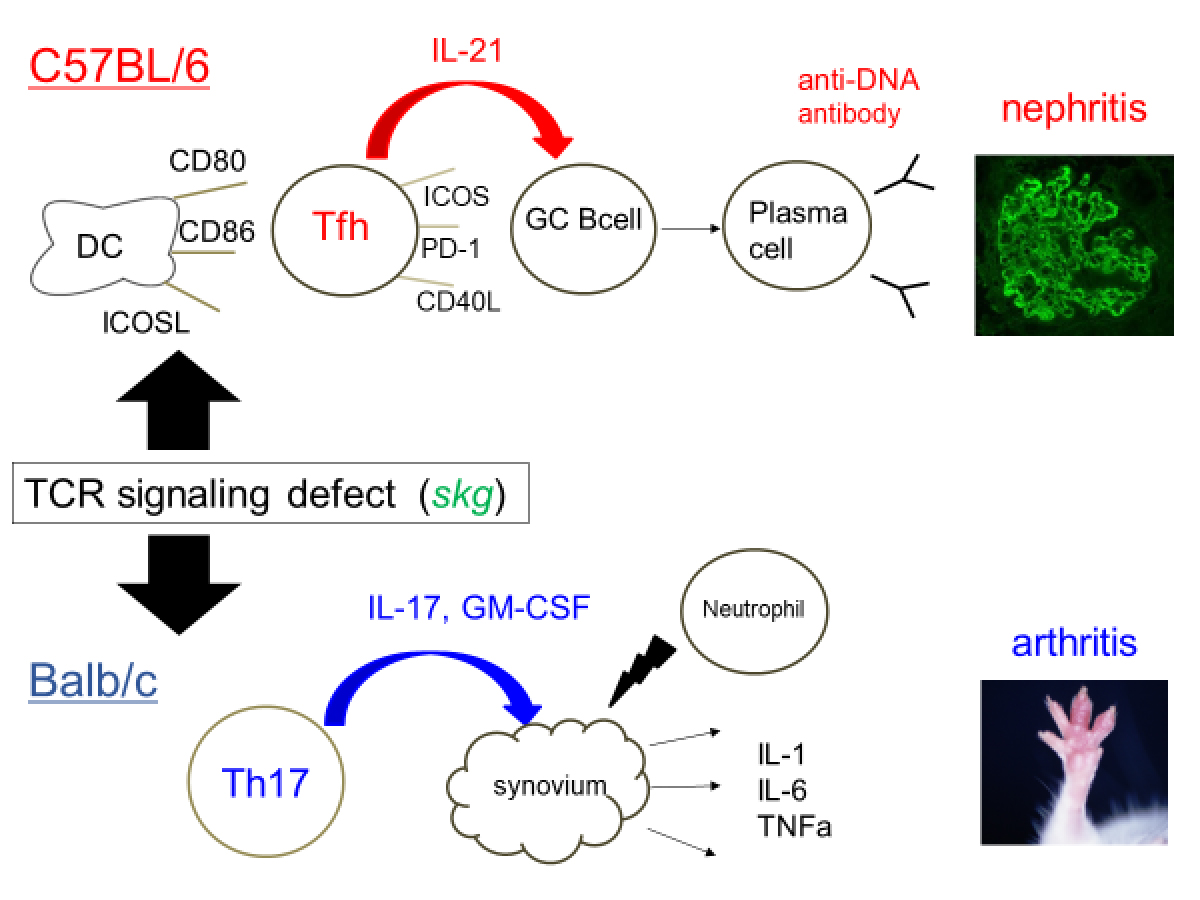
私たちは、SKGマウスというZAP70の点突然変異の結果、遺伝・環境因子によって種々の自己免疫疾患を発症する動物モデルを用いて研究を行っています(1)。SKGマウスはBALB/c背景下では関節リウマチ(RA)様の関節炎を発症し、私たちはこの関節炎発症に、IL-17を産生するヘルパーT細胞(Th17)や自然免疫刺激、サイトカインGM-CSFなどが重要な役割を果たすことを示してきました(2、3、4)。また、このマウスから関節リウマチのT細胞が認識する自己抗原の一つを同定しました(5)。
一方、ZAP70などT細胞シグナル伝達系の異常は、ヒトでは関節リウマチよりもむしろSLEの疾患感受性遺伝子として知られています。そこで、SKGマウスの遺伝的背景をBALB/cからC57BL/6(B6)にかえると、関節炎でなくSLE病態を発症することを見出しました(B6SKGマウス)(6)。また、IL-17はヒトでは関節リウマチよりも脊椎関節炎(SpA)により強くかかわることが知られています。実際にSKGマウスにTh17分化を促進する自然免疫刺激を加えた場合、関節炎以外に乾癬様の皮疹や炎症性腸炎、虹彩炎、脊椎炎など脊椎関節炎の病態も生じます(7)。そこで、このモデルも参考に脊椎関節炎の病態解明もすすめています。SKGマウスはさらに他の膠原病も発症するため、私たちはヒトと動物モデルの異同を考えながら研究をすすめています。
-
参考文献(1)Sakaguchi N, et al. Nature 2001
(2)Hirota K, Hashimoto M, et al. J Exp Med 2007
(3)Hashimoto M, et al. J Exp Med 2010
(4)Hirota K, Hashimoto M, et al. Immunity 2018
(5)Ito Y, Hashimoto M, et al. Science 2015
(6)Matsuo T, Hashimoto M, et al. J Immunol 2019
(7)Ruutu, et al. Arthritis Rheum 2012
ヒト臨床検体を使った膠原病・関連病態の解明
ヒト末梢血単核球(PBMC)を用いた研究
当科は、ヒトPBMCを用いた解析により、血管炎、特に巨細胞性動脈炎(GCA)や高安動脈炎(TAK)の病態解明をすすめています(1)。GCA患者の単球由来樹状細胞(Mo-DC)は、健常人由来樹状細胞に比べ、免疫抑制性のPD-L1発現が低下しており、T細胞の活性化能が高く、それがGCAの病態に深く関与していることを明らかにしました(2)。この結果から、現在悪性腫瘍に用いられている免疫チェックポイント阻害薬が大型血管炎を引き起こす可能性も示唆されました。また、GCA患者の単球由来マクロファージ(Mo-Mac)は、MMP-9などの蛋白分解酵素の産生が亢進しており、血管壁の破綻を起こし、T細胞の浸潤を引き起こすこと(3)、さらには、GCA患者由来のCD4T細胞では、JAK-STAT経路が亢進しており、JAK阻害薬が大血管炎の病態改善に有効であることを証明しました(4)。今後も、ヒトPBMCと貴重な組織検体を組み合わせて、細胞内代謝など、シングルセルレベルの研究を行っていきたいと考えています。
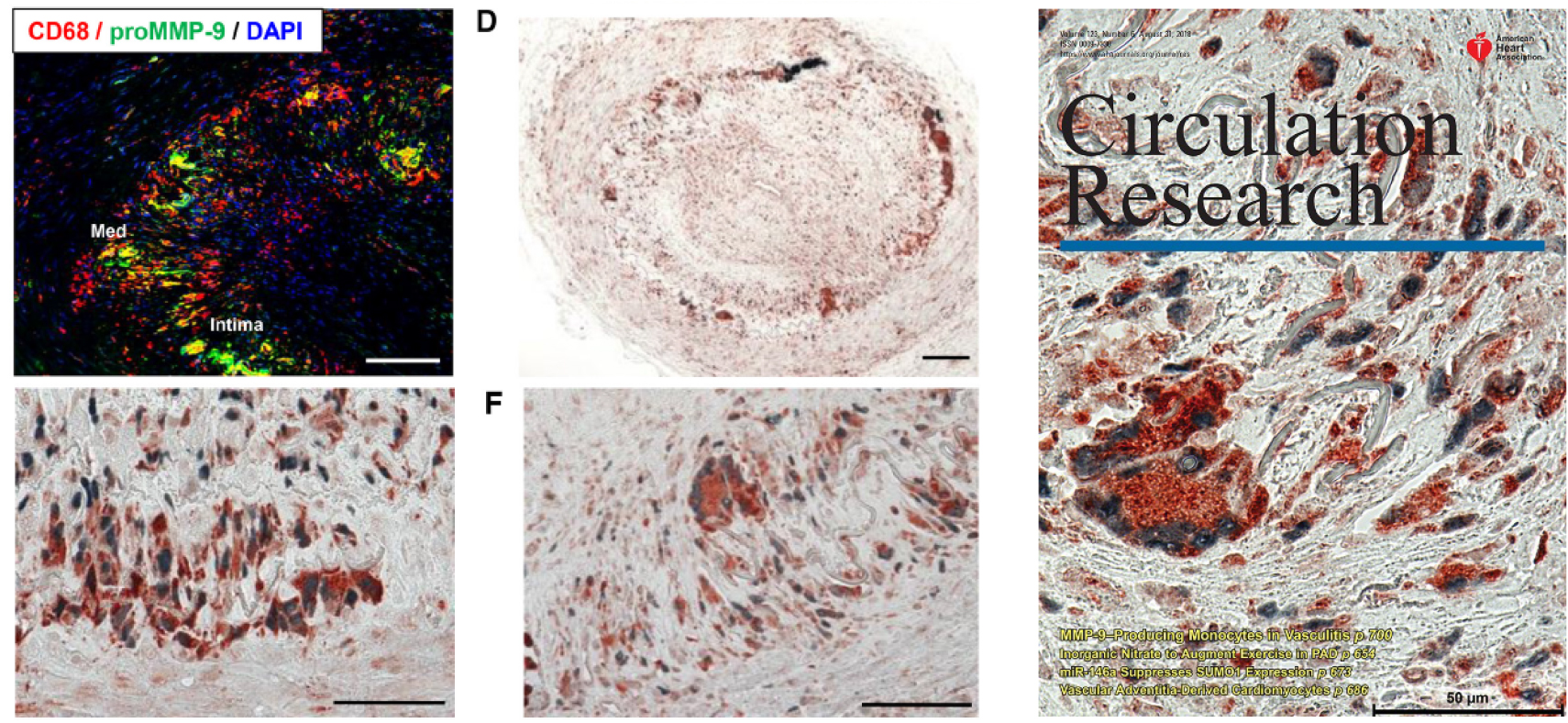
側頭動脈生検におけるMMP-9染色 Giant cellが染色されている(Circulation Research. 2018年8月の表紙に採択)
-
参考文献(1)Watanabe R, et al. Front Immunol. 2020
(2)Zhang H & Watanabe R, et al. Proc Natl Acad Sci USA. 2017
(3)Watanabe R, Maeda T, et al. Circ Res. 2018
(4)Zhang H, Watanabe R, et al. Circulation. 2018
(5)Watanabe R, et al. J Clin Invest. 2017
骨粗鬆症・サルコペニア・睡眠など患者ADLに関する研究
膠原病患者さんのADLにとって、ステロイドの副作用である骨粗鬆症やミオパチー(筋委縮)は重要な問題です。骨粗鬆症については、ビタミンD製剤やビスホスホネートに加えて、RANKL阻害薬、PTH製剤、抗スクレロスチン抗体など有用な薬剤が見つかってきましたが、ミオパチーについてはまだまだ有用な治療薬が見つかっていません。私たちはこれまで、骨粗鬆症データに紐づいた臨床サンプルを用いて骨代謝のメカニズムについて研究を進めてきました(1、2)。一方、サルコペニアについても調査を行い、関節リウマチ患者のサルコペニアや内臓脂肪などの臨床データに紐づいた血清などの臨床サンプルを有しています(3、4)。骨代謝と筋代謝はミオカインによって相互に影響を与えていることがわかってきていますので、今後、これらの臨床サンプルを活用して骨・筋代謝に関する研究を行っていきます。また、リウマチ膠原病患者さんでは、他にも睡眠障害など様々な問題がありますので5)、患者さんのADL改善につながる研究を行っていきたいと考えています。
-
参考文献(1)Tono N, Yamada S. et al. Sci Rep. 2019 ;9(1):2207.
(2)Yamada S. et al. Clin Calcium. 2019;29(2):171-177
(3)Torii M. Hashimoto M. et al. Mod Rheumatol. 2019 ;29(4):589-595.
(4)Yoshida T. Hashimoto M. et al. Rheumatol Int. 2018 ;38(9):1679-1689.
(5)Hamamoto K. Yamada S. et al. Am J Hypertens. 2015; 29(3):340-7.
腸内細菌叢に関する研究
私たちは、動物モデルを用いた研究から、SLEなどの膠原病の発症には腸内細菌叢が重要な役割を果たすことを見出しました(Shirakashi, Hashimoto, et al. Arthritis Rheumatol 2021. In Press)。その知見をヒト臨床に応用するために、ヒト膠原病患者さんから腸内細菌叢を採取させていただき、膠原病の病態と腸内細菌叢に関するトランスレーショナルリサーチを展開しています。このような研究を行うためには、膠原病患者さんの臨床サンプルが極めて重要になるため、膠原病患者さんの疾患データベースを整備し研究をすすめていきます。また、本学では他の基礎・臨床研究室でも腸内細菌叢研究が盛んであり、本学の強みといえる研究分野のため、本研究は他の研究室とも積極的に連携して研究を展開していく予定です。
研究実績
英文論文
-
Watanabe R, Hashimoto M, Murata K, Murakami K, Tanaka M, Ohmura K, Ito H and Matsuda S. Prevalence and predictive factors of difficult-to-treat rheumatoid arthritis: the KURAMA cohort. Immunol Med. 2021. In press.
- 訳)リウマチ因子が高く肺合併症のあるリウマチ患者さんは、様々な治療薬を用いても寛解を達成するのが困難であることを見出しました。
-
Kitada T, Kadoba K, Watanabe R (corresponding author), Koyama T, Nakayama Y, Taki M, Yukawa S, Odani K and Morinobu A. Listeriosis presenting with fever, arthralgia, elevated liver enzymes, hyperferritinaemia in pregnancy: a critical mimicker of adult-onset Still's disease. Scand J Rheumatol. 2021. In press.
- 訳)成人スティル病に類似した症状を呈したリステリア感染症の症例を報告しました。
-
Kadoba K, Watanabe R (corresponding author), Iwasaki T,,,, Hashimoto M, Tanaka M, Ohmura K, Morinobu A, Terao C, Yoshifuji H. A susceptibility locus in the IL12B but not LILRA3 region is associated with vascular damage in Takayasu Arteritis. Scientific Reports, 2021. In press.
- 訳)高安動脈炎の疾患感受性遺伝子として同定されたIL-12Bが、血管障害の程度と関係することを報告しました。
-
Yamada S, Inaba M. Potassium Metabolism and Management in Patients with CKD. Nutrients. 21;13(6):1751, 2021.
- 訳)慢性腎臓病におけるカリウム代謝についてレビューしました。この中で糖尿病合併例ではカリウム上昇に対する防御反応が脆弱化していることを示す自験データを報告しています。
和文論文・著書など
- 編集分担者:渡部 龍、橋本 求. 第IV章:代表的な疾患 1. 関節リウマチ ④治療(bDMARDs+tsDMARDs)ここが知りたい!膠原病診療ハンドブック, p129-138, 中外医学社, 東京, 2021.